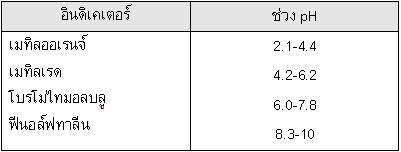
นำสารละลาย HA ซึ่งเป็นกรดอ่อนชนิดหนึ่งปริมาตร 50.00 cm3 ไปไทเทรตกับสารละลายมาตรฐาน NaOH เข้มข้น 0.15 โมล/ลิตร พบว่าเมื่อเติม NaOH ลงไป 12.00 cm3 จะทำให้สารละลายที่ได้มี pH 7 และเมื่อเติม NaOH ลงไป 16.00 cm3 จะถึงจุดยุติพอดี สารละลายกรด HA มีความเข้มข้นเริ่มต้นเท่าใด และการไทเทรตกรด-เบสคู่นี้ควรใช้อินดิเคเตอร์ชนิดใด (กำหนด Ka ของกรดอ่อน HA = 1.7 x 10-6) กำหนดให้
วิธีทำ
ที่จุดยุติจำนวนโมล NaOH = 0.1500 x mol
mol
สมมติความเข้มข้นเริ่มต้นของ HA = X โมล/ลิตร
HA + NaOH NaA + H2O
NaA + H2O
จำนวนโมล HA : NaOH = 1 : 1
เพราะฉะนั้นจำนวนโมล HA = 0.1500 x ด้วย
ด้วย
= X( )
)
X( ) = 0.1500 x
) = 0.1500 x 
X = 0.048
ความเข้มข้นเริ่มต้น = 0.048 โมล/ลิตร
เพราะฉะนั้นความเข้มข้นของ NaA = 0.048 โมล/ลิตร
การไทเทรตกรดอ่อนกับเบสแก่ที่จุดยุติ มี NaA ซึ่งแตกตัวให้ A-
A- (aq) + H2O (l) HA (aq) + OH-(aq)
HA (aq) + OH-(aq)
ความเข้มข้นเริ่มต้น 0.048 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.048-x x x

5.88 x 10-9 =
1.4 x 10-5 = (
( x มีค่าน้อยมาก 0.048-x
x มีค่าน้อยมาก 0.048-x  0.048)
0.048)
x = 1.68 x 10-5 = [OH-]
pOH = -log[OH-] = -log[1.68 x 10-5] = 4.77
pH = 14 - pOH = 14 - 4.77 = 9.22
ดังนั้น ควรใช้ฟีนอล์ฟทาลีนเป็นอินดิเคเตอร์
ที่จุดยุติจำนวนโมล NaOH = 0.1500 x
สมมติความเข้มข้นเริ่มต้นของ HA = X โมล/ลิตร
HA + NaOH
จำนวนโมล HA : NaOH = 1 : 1
เพราะฉะนั้นจำนวนโมล HA = 0.1500 x
= X(
X(
X = 0.048
ความเข้มข้นเริ่มต้น = 0.048 โมล/ลิตร
เพราะฉะนั้นความเข้มข้นของ NaA = 0.048 โมล/ลิตร
การไทเทรตกรดอ่อนกับเบสแก่ที่จุดยุติ มี NaA ซึ่งแตกตัวให้ A-
A- (aq) + H2O (l)
ความเข้มข้นเริ่มต้น 0.048 0 0
ความเข้มข้นที่เปลี่ยนไป -x +x +x
ความเข้มข้นที่ภาวะสมดุล 0.048-x x x

5.88 x 10-9 =
1.4 x 10-5 =
x = 1.68 x 10-5 = [OH-]
pOH = -log[OH-] = -log[1.68 x 10-5] = 4.77
pH = 14 - pOH = 14 - 4.77 = 9.22
ดังนั้น ควรใช้ฟีนอล์ฟทาลีนเป็นอินดิเคเตอร์