ปริมาณสารสัมพันธ์ 1
ปริมาณสารสัมพันธ์ คือ ความสัมพันธ์ระหว่างมวลหรือน้ำหนักของธาตุต่าง ๆ ของสารประกอบในปฏิกิริยาเคมี
ปริมาณสารสัมพันธ์มีประโยชน์ในแง่ของการคาดคะเนปริมาณของสารที่ต้องใช้เป็นสารตั้งต้นเพื่อให้เกิดผลิตภัณฑ์ที่ต้องการ
ระบบ คือ สิ่งต่าง ๆ ที่อยู่ภายในขอบเขตที่กำลังศึกษา ส่วนที่อยู่รอบ ๆ ระบบเรียกว่า สิ่งแวดล้อม
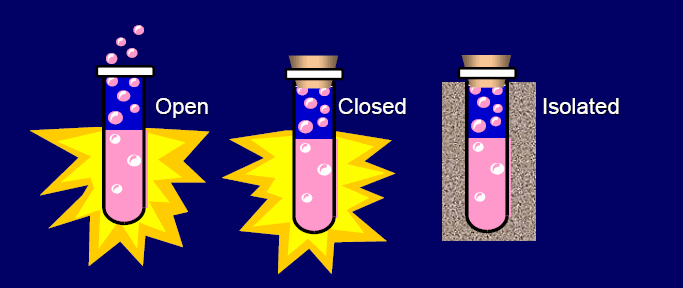
ระบบแบ่งออกเป็น 3 ชนิด คือ
1. ระบบปิด (closed system) คือ ระบบที่มีการแลกเปลี่ยนหรือถ่ายโอนพลังงานกับสิ่งแวดล้อมได้ แต่ถ่ายโอน
หรือแลกเปลี่ยนมวลกับสิ่งแวดล้อมไม่ได้ หรือมวลของระบบคงที่เมื่อเกิดการเปลี่ยนแปลง เช่น การต้มน้ำในภาชนะปิดบน
เตาไฟ ระบบคือภาชนะที่มีน้ำบรรจุอยู่ภายใน ส่วนเตาไฟและอากาศที่ล้อมรอบทั้งหมดเป็นสิ่งแวดล้อม ระบบจะรับความ
ร้อนจากเตาไฟแล้วกลายเป็นไอคายพลังงานให้กับสิ่งแวดล้อม (มีการแลกเปลี่ยนหรือถ่ายโอนพลังงาน) เมื่อชั่งน้ำหนักของ
ภาชนะที่บรรจุน้ำก่อนการต้มและหลังการต้มในภาชนะปิดจะเท่ากัน (มวลของระบบคงที่)
2. ระบบเปิด (open system) คือ ระบบที่มีการแลกเปลี่ยนหรือถ่ายโอนทั้งพลังงานและมวลให้กับสิ่งแวดล้อม หรือ
มวลของระบบไม่คงที่เมื่อเกิดการเปลี่ยนแปลง เช่น การต้มน้ำในภาชนะเปิดบนเตาไฟ ระบบคือ ภาชนะเปิดที่มีน้ำบรรจุอยู่
เตาไฟและอากาศที่ล้อมรอบทั้งหมดคือสิ่งแวดล้อม ระบบที่มีการรับความร้อนจากเตาไฟและคายความร้อนให้กับสิ่งแวดล้อม
(มีการแลกเปลี่ยนหรือถ่ายโอนพลังงาน) เมื่อชั่งน้ำหนักของภาชนะกับน้ำก่อนการต้มและหลังการต้มจะไม่เท่ากัน (มวลของ
ระบบไม่คงที่)
3. ระบบโดดเดี่ยว (แยกตัวหรือเอกเทศ) คือ ระบบที่ไม่เกิดการแลกเปลี่ยนพลังงานหรือมวลสารกับสิ่งแวดล้อม เช่น
น้ำร้อนในกระติกน้ำร้อน
3.2 กฎต่าง ๆ ที่เกี่ยวข้องกับการเปลี่ยนแปลง
3.2.1 กฎทรงมวล
อองตวน โลรอง ลาวัวซิเอ ได้ตั้งกฎทรงมวลซึ่งสรุปได้ว่า “มวลของสารทั้งหมดก่อนทำปฏิกิริยาย่อมเท่ากับมวลของสารทั้งหมดหลังทำปฏิกิริยา” กฎนี้จะใช้ได้กับปฏิกิริยาเคมีในระบบปิด ใช้ไม่ได้กับปฏิกิริยาเคมีนิวเคลียร์ เช่น เทียนไข
ในภาชนะปิดใบหนึ่ง มวลของสารทั้งหมดก่อนทำปฏิกิริยาเท่ากับมวลของเทียนไขกับภาชนะ เมื่อจุดเทียนไขในภาชนะปิดนี้
แล้วทำการชั่งมวลใหม่ มวลจะเท่าเดิม (ระบบปิด)
3.2.2 กฎสัดส่วนคงที่
โจเซฟ เพราสต์ ได้ตั้งกฎสัดส่วนคงที่ซึ่งสรุปได้ว่า “ในสารประกอบหนึ่ง ๆ ธาตุต่าง ๆ ที่เป็นองค์ประกอบ
รวมตัวกันด้วยอัตราส่วนโดยน้ำหนักที่คงที่เสมอ” โดยไม่คำนึงถึงว่าสารประกอบนั้นจะมีกำเนิดหรือเตรียมได้โดยวิธีใด
3.3 มวลอะตอม
อะตอมเป็นอนุภาคที่เล็กที่สุดของธาตุที่สามารถทำปฏิกิริยาเคมีได้ มีรัศมีของอะตอมยาวประมาณ 10-10 เมตร
อะตอมที่เบาที่สุดมีมวลประมาณ 1.6 x 10-24 กรัม อะตอมที่หนักที่สุดมีมวลประมาณ 250 เท่า ซึ่งมีค่าน้อยมาก (เป็น
ผลคูณของ 10-24) มวลอะตอมเหล่านี้จะต้องรวมกันต่อไปเป็นมวลโมเลกุล ซึ่งทำให้ยุ่งยากในการคำนวณ จึงนิยมใช้
มวลเปรียบเทียบที่เรียกว่า มวลอะตอมหรือน้ำหนักอะตอม
มวลอะตอมของธาตุ =
มวลอะตอม คือ มวลเปรียบเทียบที่บอกให้ทราบว่ามวลของธาตุ 1 อะตอมหนักเป็นกี่เท่าของมวลของ
ธาตุมาตรฐาน 1 อะตอม
มวลของธาตุ 1 อะตอม คือ มวลที่แท้จริงของอะตอมนั้น ๆ 1 อะตอม
มวลของธาตุมาตรฐาน 1 อะตอม คือ มวลของธาตุที่ถูกใช้เป็นตัวเปรียบเทียบ ซึ่งทุกอะตอมต้องมีค่าเท่ากันหมด
จึงเรียกว่ามวลมาตรฐาน มีค่าเท่ากับ 1.66 x 10-24 กรัมหรือ 1 amu (atomic mass unit)
ถ้ากำหนดให้มวลอะตอมของธาตุ H = 1 จากสูตรการหามวลอะตอมของธาตุ มวลของธาตุ H 1 อะตอม
= 1.66 x 10-24 กรัม ดังนั้นจึงเขียนสูตรใหม่ได้ดังนี้
มวลอะตอมของธาตุ =
(เพราะมวลของธาตุมาตรฐาน 1 อะตอมเท่ากับมวลของธาตุไฮโดรเจน 1 อะตอม)
ในทำนองเดียวกัน ถ้ามวลอะตอมของ C = 12 จากสูตรการหามวลอะตอมของธาตุ มวลของธาตุ C 1 อะตอม
= 12 x 1.66 x 10-24 กรัม ถ้าใช้มวลของธาตุ C 1 อะตอมเป็นค่ามาตรฐานจะได้สูตร
มวลอะตอมของธาตุ =
มวลของธาตุมาตรฐาน 1 อะตอมต้องคูณด้วย เพราะมวลของ C 1 อะตอม = 12 x 1.66 x 10-24 กรัม
ต้องทำให้มวลของธาตุมาตรฐานมีค่าเท่ากันหมด และเท่ากับ 1.66 x 10-24 กรัม
ในทำนองเดียวกัน ถ้ามวลอะตอมของ O และ N เท่ากับ 16 และ 14 ตามลำดับ จะได้สูตรดังนี้
มวลอะตอมของธาตุ =
มวลอะตอมของธาตุ =
นอกจากนี้มวลอะตอมยังคำนวณได้จากมวลเฉลี่ยของบรรดาไอโซโทปที่มีในธรรมชาติ
มวลอะตอมเฉลี่ย =
ลักษณะสำคัญของมวลอะตอม มีดังนี้
1. มวลอะตอมของธาตุไม่มีหน่วย
2. มวลอะตอมเป็นค่าเปรียบเทียบ ส่วนมวลของธาตุ 1 อะตอมเป็นมวลที่แท้จริง มีหน่วยเป็นกรัม
3. มวลของธาตุมาตรฐาน 1 อะตอม ที่ใช้เป็นตัวถูกเปรียบเทียบของมวลอะตอมมีค่าเท่ากันหมดในทุก ๆ
ธาตุ
4. คำนวณได้จากสูตรเมื่อทราบมวลของธาตุนั้น 1 อะตอม และคำนวณได้จากไอโซโทปของธาตุนั้น ๆ
การคำนวณมวลอะตอมของธาตุ
แบบที่ 1 เมื่อกำหนดมวลของธาตุ 1 อะตอม และมวลของธาตุมาตรฐาน 1 อะตอมมาให้
ตัวอย่างที่ 3.1 ธาตุ A 1 อะตอม หนัก 16 หน่วยน้ำหนัก ธาตุ 12C 1 อะตอม หนัก 12 หน่วยน้ำหนัก จงหามวล
อะตอมของธาตุ A
วิธีทำ จากสูตร มวลอะตอมของธาตุ =
=
(เมื่อใช้ธาตุ 12C 1 อะตอมเป็นธาตุมาตรฐาน)
= = 16
ดังนั้น มวลอะตอมของธาตุ A = 16 ตอบ
แบบที่ 2 เมื่อทราบมวลอะตอมของแต่ละไอโซโทปและปริมาณในธรรมชาติ
ตัวอย่างที่ 3.2 จงหามวลอะตอมเฉลี่ยของแมกนีเซียม เมื่อกำหนดมวลอะตอมและปริมาณของแต่ละไอโซโทป
มาให้ดังต่อไปนี้
ไอโซโทป | มวลอะตอม | ปริมาณในธรรมชาติ (%) |
24Mg 25Mg 26Mg | 23.9850 24.9858 25.9826 | 78.70 10.13 11.17 |
วิธีทำ มวลอะตอมเฉลี่ย =
=
= 24.310
ดังนั้น มวลอะตอมของแมกนีเซียมเท่ากับ 24.310 ตอบ
แบบที่ 3 หาจำนวนอะตอมจากมวลอะตอม
ตัวอย่างที่ 3.3 ธาตุแมกนีเซียมมีมวลอะตอม = 24 จงหาจำนวนอะตอมของธาตุแมกนีเซียม 2.4 กรัม
วิธีทำ มวลอะตอมของธาตุ =
24 =
มวลของธาตุ 1 อะตอม = 24 x 1.66 x 10-24 กรัม
หรือ ธาตุ Mg 24 x 1.66 x 10-24 g คิดเป็น = 1 atom
ธาตุ Mg 2.4 g คิดเป็น =
= 6.02 x 1022 atom
ดังนั้น ธาตุแมกนีเซียม 2.4 กรัมมี 6.02 x 1022 อะตอม ตอบ
3.4 ขนาดโมเลกุล
โมเลกุล คือ หน่วยโครงสร้างที่เล็กที่สุดของธาตุที่สารประกอบที่สามารถอยู่ได้เป็นอิสระ และยังคงแสดงสมบัติ
ของธาตุหรือสารประกอบนั้น ๆ โดยสมบูรณ์ โมเลกุลเกิดจากอะตอมรวมกัน
โมเลกุลไม่สามารถมองเห็นได้ด้วยตาเปล่าจึงทำให้การประมาณขนาดโมเลกุลยุ่งยาก เราจึงสมมติให้โมเลกุล
เป็นวัตถุที่สามารถมองเห็นได้ด้วยตาเปล่าได้
สมมติให้โมเลกุล 1 โมเลกุลคือลูกเต๋า 1 ลูก (เมื่อโมเลกุลเป็นรูปลูกบาศก์) นำเอาลูกเต๋าหลาย ๆ ลูกมาเรียงตัว
เป็นชั้นเดียว จะพบว่า
ความสูงของชั้น = ด้าน 1 ด้านของลูกเต๋า 1 ลูก
= ด้าน 1 ด้านของโมเลกุล (เมื่อโมเลกุลเป็นรูปลูกบาศก์)
จากสูตร ปริมาตรของรูปสี่เหลี่ยมลูกบาศก์ = (ด้าน)3
ดังนั้น ปริมาตรของ 1 โมเลกุล = (ความสูงของชั้น)3
สมมติให้ลูกแก้ว 1 ลูก คือโมเลกุล 1 โมเลกุล (เมื่อโมเลกุลเป็นรูปทรงกลม) นำเอาลูกแก้วหลาย ๆ ลูกมาเรียง
ตัวเป็นชั้นเดียว จะพบว่า
ความสูงของชั้น = เส้นผ่านศูนย์กลางของลูกแก้ว 1 ลูก
= เส้นผ่านศูนย์กลางของโมเลกุล 1 โมเลกุล
จากสูตร ปริมาตรของทรงกลม = เมื่อ r คือรัศมีของรูปทรงกลม
ปริมาตรของ 1 โมเลกุล =
=
จะเห็นได้ว่าเมื่อโมเลกุลเป็นรูปลูกบาศก์หรือรูปทรงกลมจะต้องใช้ความสูงของชั้นในการคำนวณในสูตรต่าง ๆ
ดังนั้น ถ้าเราสามารถหาความสูงของชั้นได้ เราจะหาขนาดของโมเลกุลได้ ความสูงของชั้นอาจหาได้จากปริมาตรรวม
ดังสูตร
ปริมาตรรวม = พื้นที่หน้าตัด x ความสูงของชั้น
ในการหาขนาดโมเลกุลของกรดโอเลอิกโดยประมาณทำได้โดยโรยผงชอล็กบาง ๆ ลงบนผิวน้ำในถาดแล้วหยด
สารละลายกรดโอเลอิกในเอทานอลลงไป 1 หยด
ความเข้มข้นของสารละลายกรดโอเลอิกในเอทานอล a เปอร์เซ็นต์โดยปริมาตร
เส้นผ่านศูนย์กลางของวงที่หยดลงแผ่ออกได้ d เซนติเมตร
สารละลายกรดโอเลอิก 1 ลูกบาศก์เซนติเมตร มี x หยด
สมมติให้โมเลกุลของกรดโอเลอิกเรียงตัวกันเป็นแผ่นฟิล์มบาง ๆ ชั้นเดียว จงหาปริมาตรของ 1 โมเลกุลโดยประมาณ
เมื่อโมเลกุลเป็นรูปลูกบาศก์หรือรูปทรงกลม
หารปริมาตรรวม
ในสารละลายกรดโอเลอิก x หยด คิดเป็น 1 cm3
ในสารละลายกรดโอเลอิก 1 หยด คิดเป็น cm3
ความเข้มข้นของสารละลายกรดโอเลอิก a เปอร์เซ็นต์โดยปริมาตร
ในการละลายกรดโอเลอิก 100 cm3 มีกรดโอเลอิก = a cm3
ในสารละลายกรดโอเลอิก cm3 มีกรดโอเลอิก = cm3
หาพื้นที่หน้าตัด
เมื่อหยดกรดโอเลอิกลงบนน้ำในถาด พื้นที่หน้าตัดจะเป็นวงกลม
สูตรของพื้นที่วงกลม
พื้นที่วงกลม =
เส้นผ่าศูนย์กลางของวงแผ่ออกได้ 2 cm3
พื้นที่หน้าตัด =
=
หาความสูงของชั้น
ปริมาตรรวม = ความสูงของชั้น x พื้นที่หน้าตัด
= ความสูงของชั้น x
ความสูงของชั้น =
เมื่อโมเลกุลเป็นรูปลูกบาศก์
ปริมาตร 1 โมเลกุล (โดยประมาณ) =
เมื่อโมเลกุลเป็นรูปทรงกลม
ปริมาตรของ 1 โมเลกุล (โดยประมาณ) =
3.5 มวลโมเลกุล
เนื่องจากโมเลกุลมีขนาดเล็กมากเช่นเดียวกับอะตอม ดังนั้น มวลของโมเลกุลจึงนิยมบอกเป็นค่าเปรียบเทียบ
เช่นกัน
มวลโมเลกุลของสาร =
=
=
3.5.1 ลักษณะสำคัญของมวลโมเลกุล
1. มวลโมเลกุลไม่มีหน่วย เพราะเป็นค่าเปรียบเทียบกับค่ามาตรฐาน
2. มวลของสาร 1 โมเลกุล คือมวลที่แท้จริงของโมเลกุลนั้น ๆ 1 โมเลกุล
3. มวลโมเลกุลคำนวณได้จากมวลอะตอมรวมกัน เพราะโมเลกุลเกิดจากอะตอมรวมกัน หรือได้จากมวลของสาร
1 โมเลกุล เปรียบเทียบค่ามาตรฐาน
4. มวลมาตรฐานที่ถูกเปรียบเทียบต้องมีค่าเท่ากันหมดในทุก ๆ โมเลกุล
3.5.2 การคำนวณมวลโมเลกุลของสาร
แบบที่ 1 เมื่อรู้มวลอะตอมของอะตอมที่ประกอบกันเป็นโมเลกุล
มวลโมเลกุลของสาร = มวลอะตอมของธาตุในโมเลกุลรวมกัน
ตัวอย่างที่ 3.4 จงหามวลโมเลกุลของ CaSO4 . 2H2O กำหนดมวลอะตอมของ Ca = 40, S = 32, O = 16 และ H = 1
วิธีทำ มวลโมเลกุลของ CaSO4 . 2H2O = มวลอะตอมของทุกธาตุใน CaSO4 . 2H2O รวมกัน
= 40+32+(16 x 4)+2(2)+2(16)
= 40+32+64+4+32 = 172
ดังนั้น มวลโมเลกุลของ CaSO4 . 2H2O = 172 ตอบ
แบบที่ 2 เมื่อทราบมวลของสาร 1 โมเลกุล และมวลของธาตุมาตรฐาน 1 อะตอม
ตัวอย่างที่ 3.5 จงหามวลโมเลกุลของออกไซด์ของธาตุ X เมื่อออกไซด์ของธาตุ X 10 โมเลกุล หนัก a กรัมและมวลของ
12C 1 อะตอม หนัก b กรัม
วิธีทำ ออกไซด์ของธาตุ X 1 โมเลกุล หนัก = กรัม
มวลโมเลกุลของออกไซด์ของธาตุ X =
=
=
ดังนั้น มวลโมเลกุลของออกไซด์ของธาตุ X = ตอบ
นอกจากนี้ยังมีการหาโมเลกุลได้จากวิธีอื่น ๆ อีก เช่น หาจากโมลหรือจากกฎของอาโวกาโดร เป็นต้น
3.6 โมล
โมล คือ หน่วยของปริมาณสารหน่วยหนึ่งที่มีความหมายเช่นเดียวกับกรัมโมเลกุล กรัมอะตอมหรือกรัม
ไอออน มีวิธีหาได้ 4 แบบ ดังต่อไปนี้
3.6.1 จำนวนอนุภาคต่อโมลของสาร
สสารทุกชนิด 1 โมลมีจำนวน 6.023 x 1023 อนุภาค (6.023 x 1023 คือเลขอาโวกาโดร)
อนุภาค คือ อะตอมโมเลกุล ไอออน อิเล็กตรอน เป็นต้น
- ธาตุ เช่น Na 1 โมล มีจำนวน 6.023 x 1023 โมเลกุล หรือ 6.023 x 1023 อะตอม
Na+ 1 โมล มีจำนวน 6.023 x 1023 ไอออน
Cl2 1 โมล มีจำนวน 6.023 x 1023 โมเลกุล หรือ 2 x 6.023 x 1023 อะตอม ( 1 โมเลกุลมี 2 อะตอม),
Cl- 1 โมล มีจำนวน 6.023 x 1023 ไอออน
- สารประกอบ เช่น SO3 1 โมล มีจำนวน 6.023 x 1023 โมเลกุล หรือ 4 x 6.023 x 1023 อะตอม
(SO3 1 โมเลกุลประกอบด้วย H 2 อะตอม S 1 อะตอม และ O 4 อะตอม รวมเป็น 7 อะตอม)
3.6.2 จำนวนโมลกับมวลของสาร
โมล =
โมล =
1 =
มวลโมเลกุลหรือมวลอะตอม = มวล(กรัม)
ดังนั้น มวลหรือน้ำหนักของสาร 1 โมล คือมวลโมเลกุลหรือมวลอะตอม ตัวอย่างเช่น O2 1 โมล หนัก 32 กรัม
จงหามวลโมเลกุลของก๊าซออกซิเจน เมื่อกำหนดให้มวลอะตอมของ O = 16
โมล =
1 =
ดังนั้น มวลโมเลกุลของก๊าซออกซิเจน = 32
จะเห็นว่ามวลโมเลกุลของก๊าซออกซิเจนมีค่าเท่ากับน้ำหนักของก๊าซออกซิเจน
3.6.3 ปริมาตรต่อโมลของก๊าซ
ก๊าซทุกชนิด 1 โมล มี 22.4 ลูกบาศก์เซนติเมตรที่ STP คือที่อุณหภูมิและความดันมาตรฐาน (ที่ 0 องศาเซลเซียส
1 บรรยากาศ หรือ 273 เคลวิน 760 มิลลิเมตรของปรอท)
ตัวอย่างเช่นไอน้ำ 1 โมล มีปริมาตร 22.4 ลูกบาศก์เดซิเมตร ที่ STP
3.6.4 ความสัมพันธ์ระหว่างจำนวนโมล อนุภาค มวล และปริมาตร
สาร 1 โมลจะมีมวลเป็นกรัมเท่ากับมวลอะตอมและมีจำนวนอนุภาคเท่ากับ 6.023 x 1023 อนุภาค และถ้าสารนั้น
เป็นก๊าซที่ STP จะมีปริมาตรเท่ากับ 22.4 ลูกบาศก์เดซิเมตร
ตัวอย่างเช่น ไอน้ำ 18 กรัมมีปริมาตร 22.4 ลูกบาศก์เซนติเมตร ที่ STP มีจำนวนอนุภาคเท่ากับ 6.023 x 1023
อนุภาค
ตัวอย่างที่ 3.6 จงหาปริมาตรที่ STP ของก๊าซไฮโดรเจนคลอไรด์ (HCl) 7.3 กรัม
โมล =
=
ก๊าซ HCl 1 โมล มีปริมาตร 22.4 dm3 ที่ STP
ก๊าซ HCl 0.2 โมล มีปริมาตร 22.4 x 0.2 = 4.48 dm3 ที่ STP
ดังนั้น ก๊าซไฮโดรเจนคลอไรด์ 7.3 g มีปริมาตร 4.48 dm3 ที่ STP
3.6.5 กฎของอาโวกาโดร
โมลของก๊าซหาได้จากกฎของอาโวกาโดร กฎของอาโวกาโดรสรุปว่า “ภายใต้เงื่อนไขเดียวกัน (อุณหภูมิและความดัน)
ก๊าซทุกชนิดที่มีปริมาตรเท่ากันจะมีจำนวนโมเลกุลและจำนวนโมลเท่ากัน เช่น ก๊าซออกซิเจน 1 ลูกบาศก์เดซิเมตร จะมีจำนวน
โมลและโมเลกุลเท่ากับก๊าซไฮโดรเจน 1 ลูกบาศก์เดซิเมตร ที่อุณหภูมิและความดันเดียวกัน และยังเท่ากับจำนวนโมลและโมเลกุลชองก๊าซอื่น ๆ ที่มีปริมาตรเท่ากันภายใต้อุณหภูมิและความดันเดียวกัน
ตัวอย่างที่ 3.7 ที่สภาวะมาตรฐาน ก๊าซออกซิเจน 1 ลูกบาศก์เดซิเมตร หนัก 1.43 กรัม และก๊าซคาร์บอนมอนอกไซด์ 1
ลูกบาศก์เดซิเมตร หนัก 1.25 กรัม จงหามวลโมเลกุลของก๊าซคาร์บอนมอนอกไซด์
วิธีทำ จากกฎของอาโวกาโดร ก๊าซออกซิเจนและก๊าซคาร์บอนมอนอกไซด์มีปริมาตรเท่ากันที่สภาวะมาตรฐานเหมือนกัน
มีจำนวนโมลและโมเลกุลเท่ากัน
จำนวนโมลของก๊าซคาร์บอนมอนอกไซด์ = จำนวนโมลของก๊าซออกซิเจน
=
=
=
ดังนั้น มวลโมเลกุลของก๊าซคาร์บอนมอนอกไซด์ = 28 ตอบ
3.7 สูตรเคมีและสมการเคมี
จำนวนโมลหาได้จากกฎของเกย์-ลูสแซกและกฎของอาโวกาโดร การหาจำนวนโมลโดยวิธีนี้เป็นการหาจำนวนโมล
ของสมการเคมี
กฎของเกย์-ลูสแซกสรุปว่า “ปริมาตรของก๊าซที่ทำปฏิกิริยากันและที่ได้จากปฏิกิริยาจะเป็นอัตราส่วนลงตัวน้อย ๆ
ที่อุณหภูมิและความดันเดียวกัน”
ตัวอย่างเช่น ก๊าซไนโตรเจน (N2) 10 ลูกบาศก์เดซิเมตร ทำปฏิกิริยาพอดีกับก๊าซไฮโดรเจน (H2) 30
ลูกบาศก์เดซิเมตรจะเกิดก๊าซแอมโมเนีย (NH3) 20 ลูกบาศก์เดซิเมตร
10 30 20 dm3 กฎของเกย์-ลูสแซก
1 3 2 dm3 (ที่อุณหภูมิและความดันเดียวกัน)
จากกฎของอาโวกาโดร : ที่อุณหภูมิและความดันเดียวกัน
ถ้า N2(g) 1 dm3 คิดเป็น 1 โมลหรือ 1 โมเลกุล
H2(g) 1 dm3 คิดเป็น 1 โมลหรือ 1 โมเลกุล
H2(g) 3 dm3 คิดเป็น 3 โมลหรือ 3 โมเลกุล
NH3 1 dm3 คิดเป็น 1 โมลหรือ 1 โมเลกุล
NH3(g) 2 dm3 คิดเป็น 2 โมลหรือ 2 โมเลกุล
1 3 2 โมล (โมเลกุล) กฎของอาโวกาโดร
(ที่อุณหภูมิและความดันเดียวกัน)
จากกฎของเกย์-ลูกแซกและกฎของอาโวกาโดร สรุปได้ว่า อัตราส่วนอย่างต่ำ (โดยปริมาตร) ของก๊าซที่เข้าทำ
ปฏิกิริยากันและที่ได้จากปฏิกิริยาจะเท่ากับจำนวนโมลหรือจำนวนโมเลกุลของก๊าซนั้น
ลักษณะสำคัญของกฎของเกย์-ลูสแซกและกฎของอาโวกาโดร
1. จำนวนโมลและโมเลกุลของสมการเคมีจะมีค่าเท่ากับปริมาตรของก๊าซที่เข้าทำปฏิกิริยาพอดีกันนั่นเอง
2. จำนวนโมลเหล่านี้คือตัวเลขที่ใช้ในการดุลสมการเคมี
3. จากปริมาตรของก๊าซที่ทำปฏิกิริยาพอดีกันและที่ได้จากปฏิกิริยาที่อุณหภูมิและความดันเดียวกัน สามารถนำ
ไปใช้หาสูตรโมเลกุลของก๊าซได้ โดยอาศัยหลักการดุลสมการเคมี
ตัวอย่างที่ 3.8 ก๊าซ X 15 ลูกบาศก์เซนติเมตร ทำปฏิกิริยาพอดีกับก๊าซ Y 45 ลูกบาศก์เซนติเมตร เกิดก๊าซ Z เพียงอย่างเดียว
30 ลูกบาศก์เซนติเมตร ปริมาตรของก๊าซทั้งหมดวัดที่อุณหภูมิและความดันเดียวกัน จงหาสูตรโมเลกุลของก๊าซ Z
วิธีทำ เมื่อก๊าซ X และ Y ทำปฏิกิริยากันได้ก๊าซ Z เพียงอย่างเดียว ดังนั้น ก๊าซ Z จะต้องมีธาตุ X และ Y เป็นองค์ประกอบ
ดังสมการ
15 45 30 cm3 (จากกฎเกย์-ลูสแซก)
1 3 2 cm3 (ที่อุณหภูมิและความดันเดียวกัน)
1 3 2 mol (จากกฎอาโวกาโดร ที่อุณหภูมิและ
ความดันเดียวกัน)
เมื่อดุลสมการเคมี จำนวนอะตอมทั้ง 2 ข้างต้องเท่ากัน a = 1, b = 3
ดังนั้น สูตรของ Z คือ XY3 ตอบ
4. จากสมการแสดงปฏิกิริยาเคมีของก๊าซที่ดุลแล้ว อัตราส่วนจำนวนโมลหรือจำนวนโมเลกุลจะเท่ากับอัตราส่วน
โดยปริมาตรของก๊าซที่เข้าทำปฏิกิริยากันและที่ได้จากปฏิกิริยา สามารถนำไปใช้หาปริมาตรของก๊าซต่าง ๆ ในปฏิกิริยาเคมี
นั้น ๆ ได้
ตัวอย่างที่ 3.9 ก๊าซผสมระหว่างก๊าซมีเทน (CH4) กับก๊าซโพรเพน (C3H8) อย่างละ 15 ลูกบาศก์เซนติเมตร จะต้องใช้ก๊าซ
ออกซิเจนกี่ลูกบาศก์เซนติเมตรจึงจะทำปฏิกิริยาพอดีกับก๊าซผสมนี้ กำหนดสมการเคมีของปฏิกิริยาเคมีดังนี้
CH4(g) + O2(g) H2O(g) + CO2(g) …………..(1)
C3H8(g) + O2(g) H2O(g) + CO2(g) …………..(2)
วิธีทำ จากสมการ (1) ดุลสมการได้ดังนี้
1 2 2 1 mol กฎอาโวกาโดร
1 2 2 1 mol และกฎเกย์-ลูสแซก
CH4 1 cm3 ทำปฏิกิริยาพอดีกับก๊าซออกซิเจน = 2 cm3
CH4 15 cm3 ทำปฏิกิริยาพอดีกับก๊าซออกซิเจน = 15 x 2 = 30 cm3
จาก (2) ;
1 5 4 3 mol
1 5 4 3 cm3
C3H8 1 cm3 ทำปฏิกิริยาพอดีกับก๊าซออกซิเจน = 5 cm3
C3H8 15 cm3 ทำปฏิกิริยาพอดีกับก๊าซออกซิเจน = 15 x 5 = 75 cm3
ต้องใช้ก๊าซออกซิเจนทั้งหมด = 30 = 75 = 105 cm3 ตอบ
ไม่มีความคิดเห็น:
แสดงความคิดเห็น